
Новый Эталон Килограмма
может в ближайшее время заменить устаревший платиново-иридиевый... »»»

Солнце Становится Ближе
получены изображения высокого разрешения Солнца с космической обсерватории Solar Dynamics Observatory... »»»

Человек "Искрививший" Время
биография Альберта Эйнштейна - величайшего физика создавшего "Общую теорию относительности"... »»»

Что за Очки у Будущего?
история создания, развития и будущее популярного оптического прибора... »»»
Определение плотности жидкостей и газа

Определение плотности жидкости
Определите массу m1чистого сухого сосуда при помощи весов, как показано на рисунке 2.6. Наполните измерительный цилиндр, пипетку или бюретку жидкостью, которую вы исследуете, и налейте ее (например, объемом 50 или 100 см3) в сосуд. Используя весы, определите массу m сосуда и жидкости. Подсчитайте массу m жидкости: m = m2— m1, а затем плотность жидкости по формуле:
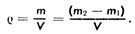
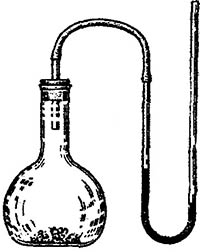
Хотя воздух представляет собой смесь газов, он подойдет для демонстрации опыта, изучаемого в этом задании. Закройте толстостенную литровую колбу резиновой пробкой и коротким отрезком трубки, снабженной зажимом Гоффмана (рис. 2.7).
«Порожняя» колба, по сути, не является таковой: она наполнена воздухом под давлением и при температуре лаборатории. При помощи весов определите массу m1 колбы с присоединенными к ней предметами. Подсоедините трубку к вакуумному насосу хорошего качества. Затем включите насос и позвольте ему выкачивать в течение нескольких минут воздух из колбы. Закрутите зажим перед выключением насоса и отсоединением трубки от него. Поскольку колба теперь почти пуста, ее масса будет меньше исходной на величину, равную массе m выкачанного воздуха.
Плотность жидкостей и газа
Плотность жидкостей
Плотности большинства жидкостей находятся в диапазоне от 0,7 до 1,3 г-см-3 (700—1300 кг-м-3), исключение составляет ртуть, поскольку она является жидким металлом, ее плотность составляет 13,6 г-см-3, т. е. довольно высока.
Плотность газа
Чтобы определить плотность газа, необходимо измерить его массу m и объем V. Однако нелегко измерить каждую из этих величин с достаточной точностью. Масса воздуха в объеме, равном 1000 см3; составляет всего лишь около 1,3 г, и, следовательно, для большей точности нужно измерять большой объем газа. Поскольку для содержания «большого» объема газа нужен и «большой» контейнер, то, скорее всего, масса контейнера поглотит массу газа, который в нем содержится, если только не применить высокоточные весы. Рычажные весы здесь не подойдут. Нужно использовать высокоточные весы, которые дают показания с точностью до 0,01 г и верхний предел которых позволяет определить массу контейнера.
Для этого эксперимента необходимо зафиксировать атмосферное давление и температуру воздуха в лаборатории. Увеличение (или уменьшение) давления на газ уменьшает (или увеличивает) его объем.
Диффузия в жидкостях и газах
 Налейте некоторое количество насыщенного (темно-голубого) раствора медного купороса в высокий лабораторный стакан. При растворении кристаллов медного купороса (соли) в воде происходит распад его на ионы Cu2+ и SO2-4 . Ионы Cu2+ ответственны за голубую окраску раствора. Затем осторожно с помощью пипетки налейте поверх раствора медного купороса слой воды.
Налейте некоторое количество насыщенного (темно-голубого) раствора медного купороса в высокий лабораторный стакан. При растворении кристаллов медного купороса (соли) в воде происходит распад его на ионы Cu2+ и SO2-4 . Ионы Cu2+ ответственны за голубую окраску раствора. Затем осторожно с помощью пипетки налейте поверх раствора медного купороса слой воды.
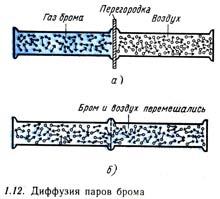
Накройте стакан бумажным фильтром и не прикасайтесь к нему несколько дней. В первоначальный момент водный слой будет находиться над раствором медного купороса (рис. 1.11, а), поскольку он менее плотен. Однако со временем пограничная линия начнет довольно быстро исчезать, и через несколько дней раствор станет однородного бледно-голубого цвета (рис. 1.11, б).
Твердые тела, жидкости и газы
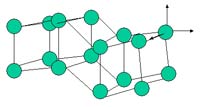
Твердые тела
Согласно молекулярно-кинетической теории вещество состоит из мельчайших частиц (молекул, атомов или ионов), стабильность которых поддерживают внутримолекулярные силы. В твердом теле эти силы достаточно велики для того, чтобы удержать молекулы вместе, придавая этому веществу его жесткую форму. Молекулы в твердом теле совершают непрерывное колебательное движение около некоторого среднего положения. Они не перемещаются внутри объема твердого тела. По мере повышения температуры амплитуда колебаний молекул увеличивается, а вместе с тем возрастает число молекул, оторвавшихся от среднего положения, вокруг которого они совершали колебания.
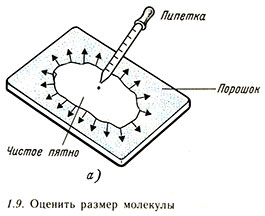
Определение размера молекулы. Движение молекул в жидкостях и газах
Приготовьте раствор олеиновой кислоты в спирте определенной концентрации, например 1 см3кислоты в 1000 см3 раствора. Этим раствором наполните градуированную по 1 см3 пипетку и определите число капель, содержащееся в 1 см3этого раствора. Подсчитайте число капель в 1 см3несколько раз и выведите среднее число n. Таким образом, среднее значение объема, соответствующего одной капле, равно 1/n см3. Объем, занимаемый олеиновой кислотой в одной капле, составит 1/С х 1/n см3.
Наполните большой чистый сосуд почти до краев водой и слегка посыпьте ее поверхность ликоподиевым порошком. Держа пипетку непосредственно над поверхностью воды, осторожно капните одну каплю раствора в центр водной поверхности. Смесь олеиновой кислоты и спирта понижает поверхностное натяжение воды, и порошок раздвинется к краям сосуда. Спирт испаряется, оставляя постоянное пятно кислоты площадью А см2. Измерьте отчетливое пятно измерительной линейкой в двух направлениях под прямым углом. При этом вы можете рассматривать эту площадь как квадрат или прямоугольник или же относиться к ней как к кругу, подсчитав средний «радиус». Такая довольно грубая оценка площади отчетливого пятна будет достаточна для определения порядка значения линейного размера молекул. Если данный объем V кислоты растекается на максимальную площадь, то толщина образовавшейся пленки будет минимальной. Эта толщина и будет близка к среднему линейному размеру t молекулы кислоты.







