
Новый Эталон Килограмма
может в ближайшее время заменить устаревший платиново-иридиевый... »»»

Солнце Становится Ближе
получены изображения высокого разрешения Солнца с космической обсерватории Solar Dynamics Observatory... »»»

Человек "Искрививший" Время
биография Альберта Эйнштейна - величайшего физика создавшего "Общую теорию относительности"... »»»

Что за Очки у Будущего?
история создания, развития и будущее популярного оптического прибора... »»»
 Точкой плавления вещества является температура, при которой твердая и жидкая фазы вещества находятся в равновесии при определенном давлении, за которое обычно принимается нормальное атмосферное давление. Позже будет показано, что точка плавления изменяется с давлением и зависит от присутствия примесей.
Точкой плавления вещества является температура, при которой твердая и жидкая фазы вещества находятся в равновесии при определенном давлении, за которое обычно принимается нормальное атмосферное давление. Позже будет показано, что точка плавления изменяется с давлением и зависит от присутствия примесей.
Проведем исследование построив кривую охлаждения нафталина.
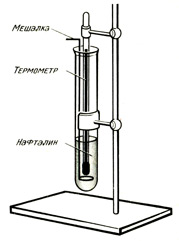
Укрепите на штативе пробирку с нафталином как показано на рисунке и затем опустите ее в лабораторный стакан с кипящей водой. Когда нафталин начнет плавиться, опустите в пробирку термометр и укрепите его на штативе. Когда температура нафталина достигнет примерно 95 оС, выньте пробирку из кипящей воды и насухо вытрите ее внешнюю сторону.
Пустите секундомер и снимайте значения температуры нафталина через интервалы в полминуты до тех пор, пока они не станут более или менее постоянными, а затем продолжайте снимать температурные показания через интервалы в одну минуту.
 Весь эксперимент по времени занимает примерно 40 мин. В то время когда жидкость остывает, она должна быть предохранена от случайных сквозняков и ее следует размешивать с целью избежания неравномерного затвердевания. В конце эксперимента вновь нагрейте нафталин, прежде чем вынимать термометр, иначе его колба может остаться в нафталине.
Весь эксперимент по времени занимает примерно 40 мин. В то время когда жидкость остывает, она должна быть предохранена от случайных сквозняков и ее следует размешивать с целью избежания неравномерного затвердевания. В конце эксперимента вновь нагрейте нафталин, прежде чем вынимать термометр, иначе его колба может остаться в нафталине.
Начертите график зависимости температуры нафталина от времени и по горизонтальной части графика определите температуру плавления нафталина (рис. 1). Вместо нафталина в этом эксперименте может быть использован парадихлорбензил. Вы получите аналогичную кривую, но точка плавления будет гораздо ниже.
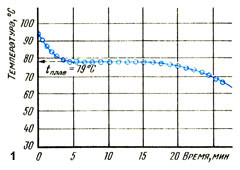
Типичная кривая охлаждения показана на рисунке 2. Рассмотрим различные части этой кривой. Кривая АВ соответствует веществу в жидком состоянии. Здесь молекулы движутся свободно в произвольных направлениях, сталкиваясь друг с другом и со стенками сосуда, в котором содержится вещество. Температура жидкости выше температуры окружающей среды, и поэтому происходит потеря тепловой энергии: температура жидкости падает. В результате молекулы теряют кинетическую энергию. Это значит, что они движутся медленнее и сближаются друг с другом.
 Кривая ВС соответствует смеси вещества в жидком и твердом состояниях. Возле точки В вещество будет преимущественно в жидком состоянии, а возле точки С - преимущественно в твердом состоянии. Поскольку температура по-прежнему выше комнатной, то тепловая энергия передается окружающей среде, но температура не падает. Это происходит потому, что тепловая энергия высвобождается изнутри вещества при его переходе из жидкого состояния в твердое. Внутренняя кинетическая энергия останется такой же, но преобразуется в энергию колебательного движения молекул. Это означает, что молекулы не будут более двигаться беспорядочно во всех направлениях, а будут колебаться вокруг фиксированного положения с одинаковой средней кинетической энергией. Потенциальная энергия уменьшится, поскольку молекулы теперь гораздо бли-же друг к другу. Вследствие этого высвобождается энергия, за счет которой поддерживается постоянная температура.
Кривая ВС соответствует смеси вещества в жидком и твердом состояниях. Возле точки В вещество будет преимущественно в жидком состоянии, а возле точки С - преимущественно в твердом состоянии. Поскольку температура по-прежнему выше комнатной, то тепловая энергия передается окружающей среде, но температура не падает. Это происходит потому, что тепловая энергия высвобождается изнутри вещества при его переходе из жидкого состояния в твердое. Внутренняя кинетическая энергия останется такой же, но преобразуется в энергию колебательного движения молекул. Это означает, что молекулы не будут более двигаться беспорядочно во всех направлениях, а будут колебаться вокруг фиксированного положения с одинаковой средней кинетической энергией. Потенциальная энергия уменьшится, поскольку молекулы теперь гораздо бли-же друг к другу. Вследствие этого высвобождается энергия, за счет которой поддерживается постоянная температура.
Кривая CD соответствует веществу в твердом состоянии. Единственным движением молекул является колебательное, и по мере высвобождения тепловой энергии кинетическая энергия колебаний уменьшается.
Проведем еще одно исследование построив кривую нагревания для воды.
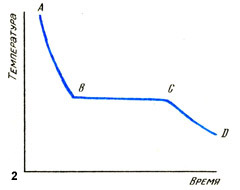
Возьмите немного льда из морозильной камеры холодильника и размельчите его в лабораторном стакане. Поместите туда термометр так, чтобы он достаточно глубоко опустился в лед, но не касался дна стакана. Нагревайте стакан снизу и снимайте значения температуры и времени каждую минуту. Изобразите графически ваши результаты. Вы должны получить кривую того типа, которая показана на рисунке 3.
 Рассмотрим участки кривой нагревания, полученной в результате исследования. Участок А В соответствует твердому состоянию — льду. При нагревании лед приобретает и потенциальную, и кинетическую энергию, и температура поднимается. Участок ВС соответствует тающему льду. Поглощенная тепловая энергия идет на увеличение потенциальной энергии молекул, которая дает им возможность двигаться хаотично. Кинетическая энергия и температура остаются постоянными. Участок CD соответствует жидкому состоянию вещества с возрастающей температурой. Здесь происходит увеличение и потенциальной, и кинетической энергий. Расстояние между отдельными молекулами возрастает, и они движутся быстрее.
Рассмотрим участки кривой нагревания, полученной в результате исследования. Участок А В соответствует твердому состоянию — льду. При нагревании лед приобретает и потенциальную, и кинетическую энергию, и температура поднимается. Участок ВС соответствует тающему льду. Поглощенная тепловая энергия идет на увеличение потенциальной энергии молекул, которая дает им возможность двигаться хаотично. Кинетическая энергия и температура остаются постоянными. Участок CD соответствует жидкому состоянию вещества с возрастающей температурой. Здесь происходит увеличение и потенциальной, и кинетической энергий. Расстояние между отдельными молекулами возрастает, и они движутся быстрее.
Участок DE соответствует смеси жидкости и пара. Температура и, следовательно, кинетическая энергия остаются постоянными до тех пор, пока вся жидкость не превратится в пар. Поглощенная теплота повышает потенциальную энергию молекул, т. е. она используется для работы, необходимой для разведения молекул врозь и превращения жидкости в пар.Дальнейшее нагревание водяного пара в закрытом пространстве даст возможность получить штриховую кривую EF. Она характеризует увеличение кинетической энергии молекул пара и его температуры.Здесь будет происходить лишь малое увеличение потенциальной энергии, поскольку молекулы слишком далеки друг от друга.
Термех - теормех решение задач готовый Яблонский, Мещерский, Тарг, шпоры







